アストラゼネカ、根治手術を受けた肺がん患者さんの術前・術後の心理状態と術後補助化学療法実施に影響を与える因子を調査
代表取締役社長:ステファン・ヴォックスストラム、 以下、 アストラゼネカ)は、
過去10年以内に肺がんの根治手術を受けたステージII-III期の肺がん患者さん(以下、 患者さん)131名を対象に、
手術前後に抱く不安や心情を理解するとともに、 患者さんが術後補助化学療法の実施を検討する際に何を重視し、 影響を受けるかを把握することを目的に、
WEBアンケート調査を実施しました。
調査結果から、 患者さんの治療選択における情報入手先として医師が80%を占めており、 術後補助化学療法実施の意思決定は、
患者さんが医師からの説明をどのように受け止めたかに大きく左右されることが明らかとなりました。 また、
患者さんは根治手術を受けたとしても再発の可能性があることを理解しており、 手術前後から術後補助化学療法実施時にいたるいずれの過程においても、
再発の可能性に不安を感じていました。 患者さんの70%が術後補助化学療法に対して、 たとえ再発時期を遅らせるだけになったとしても、
「再発を避けるためにやれることはやっておきたい」という考えを持っていることも明らかとなり、 再発までの期間の延長が、 治癒への期待や個人的な人生のイベント達成、
再発後の新たな治療法への期待などにつながっていることが考えられました。
本アンケート調査の監修をした、 広島大学 腫瘍外科 教授である岡田 守人 先生は、 次のように述べています。 「根治切除を受けた患者さんが抱える不安や、
治療選択時の希望が、 調査結果から明らかになりました。 患者さんの多くは、 生存を長くすることに加えて、 再発しない期間(DFS: Disease Free
Survival)を重要視していることがわかりました。 患者さんの希望を理解したうえで、
医師を中心とした多職種連携チームで患者さんをサポートすることがとても重要です」。
【調査概要】

調査結果の詳細レポートは下記URLよりご覧いただけます。
https://www.astrazeneca.co.jp/content/dam/az-jp/press-releases/pdf/20210511.pdf
【調査結果の概要】
医師とのコミュニケーションと患者さんの意思決定について
・ 根治手術を受けた肺がん患者さんが、 がんと診断された後に治療選択を判断する際の情報入手先は、 医師からの説明が80%であった。
患者さんの多くは医師からの説明を頼りに判断をしていた。
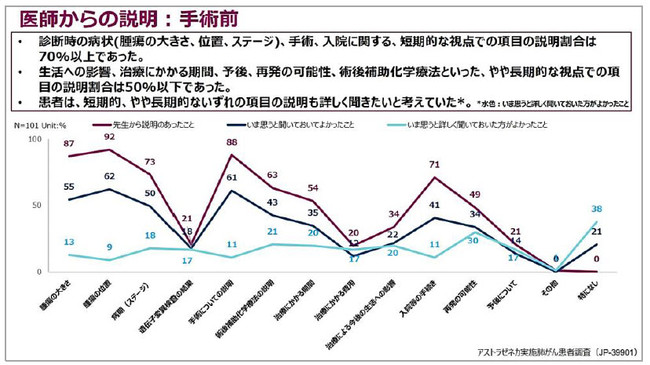
・ 医師からの説明は、 手術前後、 術後補助療法実施時のいずれにおいても、 その時点での病状や治療などの短期的な項目に関する割合が70%以上と高く、
生活への影響、 再発の可能性といったやや長期的な項目の割合は前述の項目と比べると少し低かった。 一方、
患者さんは短期的とやや長期的のいずれの項目も詳しく説明を聞きたいと考えていた。
根治手術を受けた肺がん患者さんの手術前後の心理について
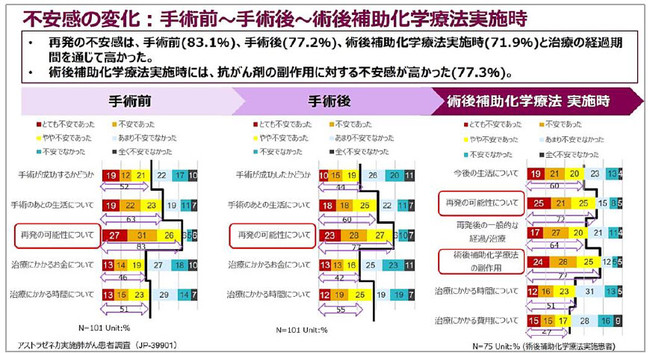
・ 患者さんは、 根治手術を受けた肺がん患者さんは、 肺がんの手術前後、 術後補助化学療法実施時のいずれの過程においても、 再発の可能性(83.1%,
77.2%, 71.9%)と今後の生活(63.4%, 60.4%, 60%)に不安を感じていた。 術後補助化学療法実施時においては、
77.3%の患者さんが副作用に対する不安を感じていた。
術後補助化学療法に対する患者さんの考えについて
・ 根治手術を受けた肺がん患者さんは医師から術後の説明として、 腫瘍のサイズ、 ステージ、 リンパ節転移の有無等を受け、 術後の病状を認識していた。
多くの患者さんはがんを切除できたとしても再発の不安を感じていた(69%)。
・ 「手術だけで治る可能性があるが、 手術だけでは再発する可能性が一定の割合ある。 術後補助化学療法によって、
再発の割合を下げることができなくても再発の時期を年単位で遅らせる可能性がある」とした場合、 「術後補助化学療法を受ける」意見に共感した患者さんは70%、
「術後補助化学療法を受けない」意見に共感した患者さんは30%であった。
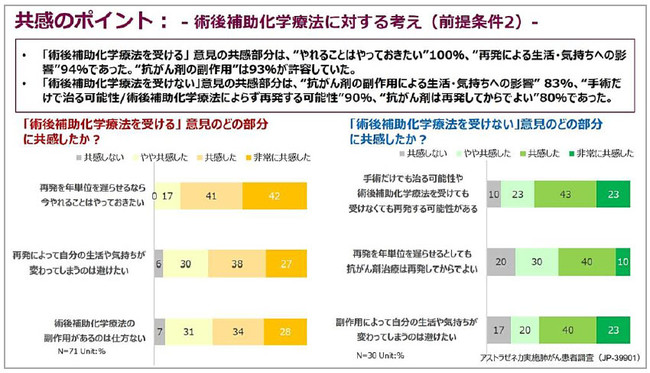
・ 「術後補助化学療法を受ける」意見に対する共感部分は、 “やれることはやっておきたい”が100%、 “再発による生活・気持ちへの影響”が94%であった。
また、 “抗がん剤の副作用”は93%が許容していた。
・ 「術後補助化学療法を受けない」意見に対する共感部分は、 “抗がん剤の副作用による生活・気持ちへの影響” が83%、
“手術だけで治る可能性/術後補助化学療法によらず再発する可能性”が90%、 “抗がん剤は再発してからでよい”が80%であった。
【考察】
・ 患者さんが診断から手術、 術後補助化学療法と治療選択の意思決定をサポートするために、 医師からの説明に加え、
適正な情報へのアクセスをサポートすることが重要と考えられた。
・ 患者さんは治療の経過を通じて、 再発への不安など様々な不安を感じており、
患者さんのサポートには医師を中心とした多職種連携チームや患者会へのアクセスが重要と考えられた。
・ 患者さんの多くは、 再発の割合を下げることができず、 再発の時期を遅らせるだけだとしても、 再発しない期間(DFS: Disease Free
Survival)を大切に考えており、 術後補助化学療法を受ける考えに共感していた。
・ 患者さんの多くは、 再発によって自分の生活や気持ちが大きく変わってしまうことを防ぐために、 やれることはやっておきたいという考えを持っており、
患者さんにとって、 普段の生活(仕事、 家庭、 人間関係、 趣味など)を送れることは、 治療に対する意思決定の重要な因子であると考えられた。
・ 患者さんにとって再発しない期間は、 治癒への期待、 個人的な人生のイベントの達成(子供の独立など)、 健康寿命の延長、
再発後の新たな治療法への期待につながっており*、 患者さんにとって重要な期間と考えられた。
* 別途、 オンライン調査回答者を対象としたインタビュー回答より
以上
*****
肺がんについて
肺がんは、 男女共にがんによる死因の第1位であり、 すべてのがんによる死亡の約5分の1を占めています(1)。 日本では、
2019年に約122,300人が肺がんと診断され、 肺がんによる死亡は約76,000人にのぼりました(2)。
肺がんは非小細胞肺がん(NSCLC)と小細胞肺がん(SCLC)に大きく分けられ、 肺がん患者さんの80~85%がNSCLCと診断されます(3)。
NSCLCの患者さんの大多数は進行がんで診断され、 切除可能と診断されるのは全体の約25~30%です(4-6)。 また早期の肺がんは、
肺がんとは無関係に撮像された画像で診断されることがほとんどです(7-8)。
切除可能ながん患者さんの多くが、 手術(腫瘍の完全切除)および術後補助療法としての化学療法を受けても再発します(9)。
肺がん領域におけるアストラゼネカについて
アストラゼネカは、 さまざまな病期における異なる組織型の肺がん、 治療法、 作用機序に対して、 承認済みおよび後期臨床開発段階の新薬候補を含め、
包括的なポートフォリオを有しています。
アストラゼネカは既承認薬イレッサ(R)(ゲフィチニブ)およびタグリッソ(R)(オシメルチニブ)の提供や、 現在進行中の第III相試験であるLAURA、
NeoADAURA、 FLAURA2によって得られる新たなエビデンスを通じて、 疾患の遺伝的要因としてのEGFR
遺伝子変異を持つ患者さんのアンメットニーズに応えることを目指しています。
また、 タグリッソとc-Met受容体チロシンキナーゼの選択的阻害薬であるサボリチニブ、 および他の新薬候補との併用療法を評価する、
現在進行中の第II相SAVANNAH試験およびORCHARD試験を通じて、 腫瘍の耐性メカニズムを解き明かそうとしています。
加えて当社の広範ながん免疫療法の開発プログラムは、 すべての肺がん患者さんの4分の3にあたる既知の遺伝子変異を持たない患者さんを対象にしています。
免疫治療ポートフォリオには、 PD-L1抗体であるイミフィンジ単剤療法、 およびトレメリムマブおよび/または化学療法との併用療法が含まれ、
病勢進行が認められた患者さんを対象とした第III相試験(POSEIDONおよびPEARL)、
治癒の可能性がある初期段階の患者さんを対象とした第III相試験(MERMAID-1, AEGEAN、 ADJUVANT BR.31、 PACIFIC-2、
PACIFIC-4、 PACIFIC-5、 およびADRIATIC)が現在進行中です。 さらに、 イミフィンジは、
まだ開発パイプラインの初期段階にある新薬候補との併用療法を評価する第II相併用投与試験(NeoCOAST、
COASTおよびHUDSON)においても検討されています。
アストラゼネカにおけるオンコロジー領域
アストラゼネカは、 あらゆる種類のがんに対して治療法を提供するという高い目標を掲げ、 がんとその発見にいたるまでの複雑さを科学に基づいて理解し、
患者さんの人生を変革する医薬品の開発および提供を通じて、 オンコロジー領域の変革をけん引していきます。
アストラゼネカは治療困難ながん種に注力しています。 当社は持続的なイノベーションにより、 医療活動および患者さんの医療経験を一変させる可能性のある、
製薬業界でもっとも多様なポートフォリオと開発パイプラインを構築しています。
アストラゼネカはがん治療のパラダイムを再定義し、 将来的にはがんによる死亡をなくすことをビジョンに掲げています。
アストラゼネカについて
アストラゼネカは、 サイエンス志向のグローバルなバイオ・医薬品企業であり、 主にオンコロジー、 循環器・腎・代謝、 および呼吸器・免疫の3つの重点領域において、
医療用医薬品の創薬、 開発、 製造およびマーケティング・営業活動に従事しています。 英国ケンブリッジを本拠地として、 当社は100カ国以上で事業を展開しており、
その革新的な医薬品は世界中で多くの患者さんに使用されています。 詳細については
https://www.astrazeneca.comまたは、 ツイッター@AstraZeneca(英語のみ)をフォローしてご覧ください。
日本においては、 主にオンコロジー、 循環器・腎・代謝、 および呼吸器・免疫を重点領域として患者さんの健康と医療の発展への更なる貢献を果たすべく活動しています。
アストラゼネカ株式会社についてはhttps://www.astrazeneca.co.jp/
https://www.astrazeneca.co.jp/
をご覧ください。
References
1. World Health Organization. International Agency for Research on Cancer. Lung
Fact Sheet. Available at
https://gco.iarc.fr/today/data/factsheets/cancers/15-Lung-fact-sheet.pdf
Accessed January 2021.
2. 公益財団法人 がん研究振興財団「がんの統計’19」
https://ganjoho.jp/data/reg_stat/statistics/brochure/2019/cancer_statistics_2019_fig_J.pdf
3. LUNGevity Foundation. Types of Lung Cancer. Available at
https://lungevity.org/for-patients-caregivers/lung-cancer-101/types-of-lung-cancer
Accessed January 2021.
4. Cagle P, et al. Lung Cancer Biomarkers: Present Status and Future
Developments. Archives Pathology Lab Med. 2013;137:1191-1198.
5. Le Chevalier T, et al. Adjuvant Chemotherapy for Resectable Non-Small-Cell
Lung Cancer: Where is it Going? Ann Oncol. 2010;21:196-8.
6. Datta D, et al. Preoperative Evaluation of Patients Undergoing Lung Resection
Surgery. Chest. 2003;123: 2096–2103.
7. Sethi S, et al. Incidental Nodule Management – Should There Be a Formal
Process?. Journal of Thorac Onc. 2016:8;S494-S497.
8. LUNGevity Foundation. Screening and Early Detection. Available at
https://lungevity.org/for-patients-caregivers/lung-cancer-101/screening-early-detection
Accessed January 2021.
9. Pignon, J.P., et al. Lung Adjuvant Cisplatin Evaluation: A Pooled Analysis by
the LACE Collaborative Group. J Clin Oncol 2008;26:3552-3559.
プレスリリースは以下よりダウンロードできます。
https://prtimes.jp/a/?f=c-24308-2021051112-5f1c0f8fc525a45f9dc1501f0cc27dd4.pdf





ディスカッション
コメント一覧
まだ、コメントがありません