-マルホと大阪大学大学院薬学研究科の共同研究-皮膚のバリア機能改善が期待できる核内受容体PPARαを活性化する有用成分を発見
マルホ株式会社(本社:大阪府大阪市北区、 代表取締役社長:杉田 淳、 以下、 マルホ)と大阪大学大学院薬学研究科(研究代表者:橘
敬祐講師)との共同研究※により、 ケラチノサイトの分化誘導、 脂質産生の促進、 バリア機能の向上、 表皮角化細胞において、
皮膚炎症の抑制などに関わる核内受容体PPARαを「ヒメガマホエキス」が活性化し、 皮膚バリア機能や保湿に関連する遺伝子発現を増加させることを明らかにしました。
ヒメガマホエキスは、 加齢や乾燥、 敏感症状などでバリア機能が低下した皮膚を健やかな状態に育む鍵となることが期待できます。
今後、 本研究成果を応用し、 角層のバリア機能を高めるスキンケア製品などの開発の検討をしてまいります。
※本研究の成果の一部はInternational Journal of Cosmetic Scienceにて論文発表しました。 【PPARαと皮膚のバリア機能】
ヒトの表皮は、 基底膜に接するケラチノサイトが分裂、 分化、 成熟することによって形成されます。 表皮には水分の蒸散を防ぐバリア機能が備わっており、
細胞間脂質がこのバリア機能に重要な役割を果たしています。 バリア機能が正常に保たれていると、 皮膚は水分を保つことができます。 しかし、
バリア機能が損なわれると乾燥などの荒れ肌の状態となります。
PPARα(ペルオキシソーム増殖剤応答性受容体α)は、 表皮に発現し、 ケラチノサイト分化の誘導、 脂質産生の促進、 バリア機能の維持、
皮膚の炎症の抑制に関与します。 PPARα活性の調整ができる物質は、 皮膚機能を制御し、 バリア機能向上が期待できます。
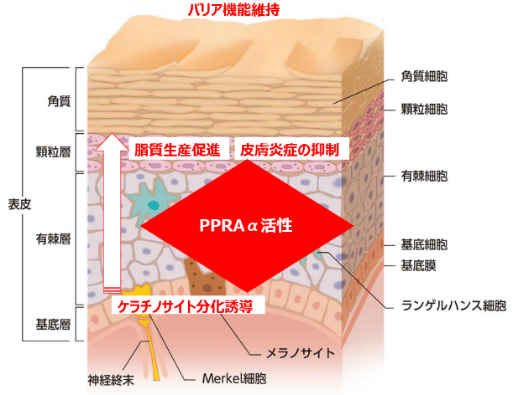
図1)PPARαは表皮に発現し、 ケラチノサイトの分化誘導、 脂質産生の促進などバリア機能の恒常性に関わっている
PPARα(ペルオキシソーム増殖剤応答性受容体α)の構造と機能(1)
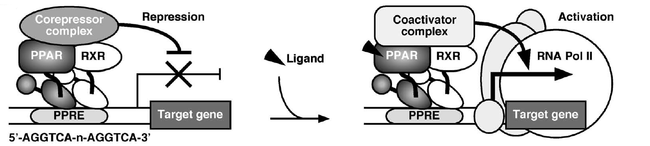
図2)PPARα(ペルオキシソーム増殖剤応答性受容体α)は核内受容体RXRとヘテロ2量体を形成することで、 DNA結合領域が標的遺伝子のPPREに結合する。
リガンド物質がリガンド結合領域に結合することで、 コアクチベーターなどと相互作用し、 標的遺伝子の発現が促進される。
リガンド物質と結合していない状態ではコリプレッサーと相互作用することで転写活性を抑制している。
【PPARαを活性化し、 バリア機能を調節するヒメガマホエキス】
大阪大学大学院薬学研究科で独自に構築されたPPARα活性化因子スクリーニング細胞株(2)を用いてスクリーニングし、
約500種類の天然エキスについてPPARα活性を評価しました。
PPARαを活性化する36種類のエキスを同定し、 その中でもヒメガマホエキスはPPARαへ特異的に作用し、 濃度依存的なPPARαの転写活性を示し(図3)、
PPARαリガンド活性成分を含むことが確認できました。
ヒメガマホエキスは、 これまで漢方の生薬として知られていましたが、 PPARαリガンド活性成分を含むことを実証したのは本研究成果が初めてです。
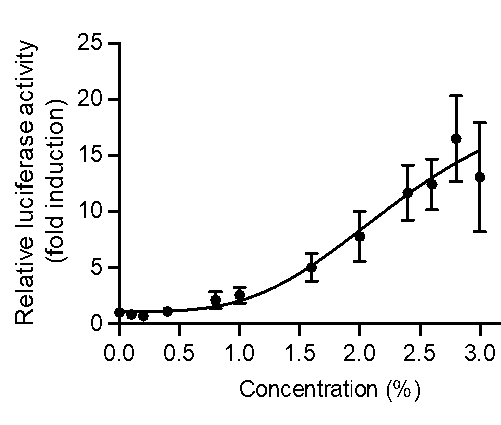
図3)濃度依存的に活性が増加している
さらに、 ヒメガマホエキスは、 正常ヒト表皮角化細胞において、 PPARα標的遺伝子ペリリピン2(PLIN2)や、
皮膚バリアや保湿に関連する遺伝子アクアポリン3(AQP3)、 ヒアルロン酸合成酵素3(HAS3)、
硫酸基転移酵素2B1b(SULT2B1b)の発現を増加させました(図4,5)

図4)PPARα標的遺伝子PLIN2
PLIN2: 皮膚の脂肪滴形成と貯蔵に関連する因子であり、 皮膚の炎症から保護する。
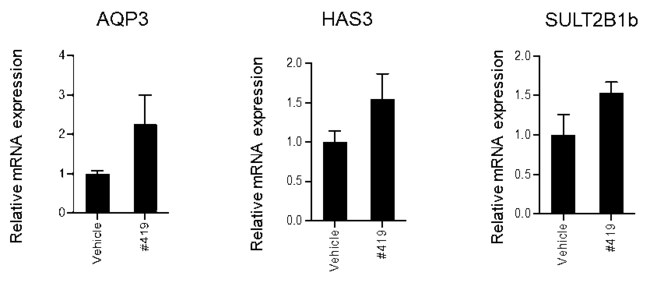
図5)ヒメガマホエキスはAQP3,HAS3,SULT2B1bの遺伝子発現を増加させている。
AQP3: 真皮から表皮へ水分子・グリセリンを輸送し、 グリセリンは表皮における脂質合成量を増加させる。
HAS3: 水分保持や組織の形態維持に関わるヒアルロン酸(HA)を合成します。 HAとヒアルロン酸レセプター(CD44)の相互作用は、
コレステロールの合成促進、 表皮角化細胞の分化誘導、 増殖促進に関与する。
SULT2B1b: バリア機能の恒常性の維持に関与する硫酸コレステロールを合成する。
PPARαの活性化は、 AQP3発現、 コレステロール硫酸合成酵素SULT2B1b発現、
HA産生の促進を介して表皮バリア脂質の一種であるコレステロールの合成促進および表皮角化細胞の分化を誘導するとともに、
脂肪滴構成因子PLIN2の発現を介してバリア機能の改善に寄与することが期待されます。
さらに、 ヒメガマホエキスと、 スクリーニングで活性のあった他のエキスとの組み合わせでのPPARα活性を確認し、
ヒメガマホエキス単体よりヒメガマホエキスと甜茶エキスの組み合わせは高いPPARα活性を示しました。
(3)PPARα活性の調整ができるヒメガマホエキスや活性のあったその他植物エキスとの組み合わせは、 バリア機能改善が期待できます。
本研究は、 日本学術振興会(JSPS)科学研究費助成金 基盤研究(B)(15H02896, 18H03190, 21H03354)、
日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業(BINDS)(JP21am0101084, JP21am0101085,
JP21am0101123)の支援を受けて行われました。
引用)
(1)Keisuke Tachibana:YAKUGAKU ZASSHI,2007;127(8),1223-1229.
(2)Keisuke Tachibana et.al.: International Journal of Biological
Chemistry,2018;293,10333‐10343.
(3)Keisuke Tachibana et.al.: International Journal of Cosmetic
Science,2022;44(2),189-200.
マルホ株式会社について
マルホ株式会社は大阪市北区に本社を置く、 医療用医薬品等の研究・開発・製造・販売を行う製薬企業です。
創業は1915年、 従業員数は1,546人(2021年9月末)です。 2021年9月期の売上高は870億33百万円でした。 “Excellence in
Dermatology”を長期ビジョンとして掲げ、 皮膚科学領域での卓越した貢献を目指しています。
マルホ株式会社についての詳細は
https://www.maruho.co.jp/をご覧くさい。
▼ ニュースリリース






ディスカッション
コメント一覧
まだ、コメントがありません